TEVIMBRA Indikationer1
Ikke småcellet lungecancer (NSCLC)
Tevimbra, i kombination med platinbaseret kemoterapi som neoadjuverende behandling og efterfulgt af monoterapi som adjuverende behandling, er indiceret til behandling af voksne patienter med resektabel NSCLC med høj risiko for recidiv.
Tevimbra, i kombination med pemetrexed og platinbaseret kemoterapi, er indiceret til førstelinjebehandling af voksne patienter med ikke-planocellulær NSCLC, hvis tumorer har PD-L1 (udtrykt på ≥ 50 % tumorceller uden EGFR- eller ALK-positive mutationer, og som har:
- lokalt fremskreden NSCLC og ikke er kandidater til kirurgisk resektion eller platinbaseret kemo‑strålebehandling, eller
- metastatisk NSCLC.
Tevimbra, i kombination med carboplatin og enten paclitaxel eller nab‑paclitaxel, er indiceret til førstelinjebehandling af voksne patienter med planocellulær NSCLC, som har:
- lokalt fremskreden NSCLC og ikke er kandidater til kirurgisk resektion eller platinbaseret kemo‑strålebehandling, eller
- metastatisk NSCLC.
Tevimbra som monoterapi er indiceret til behandling af voksne patienter med lokalt fremskreden eller metastatisk NSCLC efter tidligere platinbaseret behandling. Patienter med EGFR-mutation eller ALK-positiv NSCLC skal også have fået målrettede behandlinger, inden de får tislelizumab.
Småcellet lungecancer (SCLC)
Tevimbra, i kombination med etoposid og platinbaseret kemoterapi, er indiceret til førstelinjebehandling af voksne patienter med SCLC i et stadie med omfattende spredning.
Gastrisk adenokarcinom eller adenokarcinom i den gastroøsofageale overgang (G/GEJ)
Tevimbra, i kombination med platin- og fluoropyrimidinbaseret kemoterapi, er indiceret til førstelinjebehandling af voksne patienter med HER-2-negativ lokalt fremskreden inoperabel eller metastatisk gastrisk adenokarcinom eller adenokarcinom i den gastroøsofageale overgang (G/GEJ), hvis tumorer udtrykker PD-L1 med en tumorområde-positivitetsscore (TAP) på ≥ 5 % (se pkt. 5.1).
Øsofagealt planocellulært karcinom (OSCC)
Tevimbra, i kombination med platinbaseret kemoterapi, er indiceret til førstelinjebehandling af voksne patienter med inoperabel, lokalt fremskreden eller metastatisk OSCC, hvis tumorer udtrykker PD-L1 med en TAP-score på ≥ 5 % (se pkt. 5.1).
Tevimbra som monoterapi er indiceret til behandling af voksne patienter med inoperabelt, lokalt fremskredent eller metastatisk OSCC efter tidligere platinbaseret kemoterapi.
Nasofaryngealt karcinom (NPC)
Tevimbra, i kombination med gemcitabin og cisplatin, er indiceret til førstelinjebehandling af voksne patienter med recidiverende eller metastatisk NPC, som ikke kan behandles med helbredende kirurgi eller strålebehandling.
Reference 1: TEVIMBRA® (tislelizumab) SPC, 18.09.2025 punkt 4.1
Virkemåde for TEVIMBRA
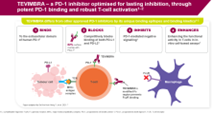
TEVIMBRA – en PD-1-hæmmer optimeret til vedvarende hæmning via potent PD-1-binding og robust T-celleaktivering1‒2
TEVIMBRA adskiller sig fra andre godkendte PD-1-hæmmere ved sine unikke bindingsepitoper og sin bindingskinetik1-2
BINDER SIG
Til det ekstracellulære domæne af humant PD-11
BLOKERER
Blokerer kompetitivt bindingen af både PD-L1 og PD-L21
82 % overfladeoverlapning
med PD-L12
HÆMMER
PD-1-medieret negativ signalering1
FORBEDRER
Forbedrer den funktionelle aktivitet i T-celler i cellebaserede in-vitro-analyser1
Need title?
- Tumorcelle
- PD-L1
- MHC: antigenkompleks
- TCR
- FcyR
- PD-1
- TEVIMBRA
- TEVIMBRAs modificerede Fc-region
forhindrer FcyR-binding
Makrofag
Need title?
- Reference 1: TEVIMBRA® (tislelizumab) SPC, 18.09.2025 punkt 5.2 2. Hong Y, et al. FEBS Open Bio. 2021;11(3):782–792
Dosering og indgivelse1
Intravenøs infusion en gang hver 3. uge ELLER hver 6. uge
Første infusion skal indgives over 60 minutter og efterfølgende infusioner over 30 minutter
200 mg pr. intravenøs infusion hver 3. uge ELLER 400 mg pr. intravenøs infusion hver 6. uge
Behandlingen bør fortsættes indtil sygdomsprogression eller uacceptabel toksicitet1
Need title?
- Reference 1: TEVIMBRA® (tislelizumab) SPC, 18.09.2025 punkt 4.2
Sikkerhedsprofil1
Sikkerheden for tislelizumab som monoterapi er baseret på samlede data fra 1.952 patienter på tværs af flere tumortyper, som fik 200 mg tislelizumab hver 3. uge. De mest almindelige bivirkninger (≥ 20 %) var anæmi, forhøjet aspartataminotransferase, træthed og forhøjet alaninaminotransferase.
De mest almindelige niveau 3/4-bivirkninger
var anæmi, forhøjet aspartataminotransferase, lungebetændelse, hyponatriæmi, forhøjet bilirubin i blodet, hypertension og træthed. 1,0 % af patienterne oplevede bivirkninger, der førte til dødsfald. De bivirkninger, der førte til dødsfald, var lungebetændelse, pneumonitis, hepatitis, trombocytopeni, dyspnø og nedsat appetit. Blandt de 1.952 patienter blev 40,7 % eksponeret for tislelizumab i over 6 måneder, og 24,7 % blev eksponeret i over 12 måneder.1
Sikkerheden for tislelizumab indgivet i kombination med kemoterapi er baseret på data fra 1.950 patienter på tværs af flere tumortyper, som fik 200 mg tislelizumab hver 3. uge, med undtagelse af forsøg BGB A317-315, hvor patienterne også fik tislelizumab i en dosis på 400 mg én gang hver 6. uge som adjuverende behandling efter neoadjuverende behandling og kirurgi. De mest almindelige bivirkninger var neutropeni, anæmi, trombocytopeni, kvalme, træthed, nedsat appetit, forhøjet alaninaminotransferase, forhøjet aspartataminotransferase, udslæt og diarré. De mest almindelige niveau 3/4-bivirkninger (≥ 2 %) var neutropeni, anæmi, trombocytopeni, hyponatriæmi, hypokaliæmi, træthed, lungebetændelse, lymfopeni, udslæt, nedsat appetit, forhøjet aspartataminotransferase og forhøjet alaninaminotransferase. 1,3 % af patienterne oplevede bivirkninger, der førte til dødsfald. De bivirkninger, der førte til dødsfald, var lungebetændelse, pneumonitis, dyspnø, myocarditis, hepatitis, trombocytopeni, 12 colitis, hypokaliæmi og myositis. Blandt de 1.952 patienter blev 40,7 % eksponeret for tislelizumab i 6 måneder eller længere, og 24,7 % blev eksponeret i 12 måneder eller længere.1
Need title?
- Reference 1: TEVIMBRA® (tislelizumab) SPC, 18.09.2025 punkt 4.8